Materia

Se
denomina materia a todo aquello que
tiene lugar en el espacio y posee una cierta cantidad de energía además de
estar sujeta a cambios en el tiempo.
Cuando
decimos que la materia tiene masa y ocupa un lugar en el espacio nos estamos refiriendo
a un tipo de materia cuantificable.
Sabemos que la ciencia que estudia
su naturaleza, composición y trasformación es la química.
Existen dos tipos de materia, ya que no toda la
materia tiene masa; así tenemos:
Materia másica: es todo aquello que ocupa un lugar
en el espacio y tiene masa básicamente es todo
aquello que podemos tocar (como el agua, la tierra, los arboles entre otros),
así como cosas que aparentemente no tocamos (como el aire).
Materia no másica: es un cierto tipo de materia que carece
de masa o por lo menos tiene una masa infinitesimalmente pequeña, aquí encontramos a los fotones pero también
se postula la existencia de otras partículas como el gravitón el fotino y el
gravitino. Gran parte de la energía del universo está compuesta por formas de
materia o campos que no presentan masa.
Composición
de la materia
La materia está integrada por átomos que
son partículas diminutas, estas a su vez se componen de otras más pequeñas que
se denominan partículas subatómicas. En el átomo podemos encontrar un núcleo y
una corteza
Núcleo
Protones: partículas subatómicas con carga
eléctrica positiva
Neutrones: partículas subatómicas sin
carga eléctrica
Pertenecen a la familia de los bariones
que son partículas subatómicas formadas por tres quarks
Corteza
Electrones: partículas subatómicas con
carga eléctrica negativa
Los átomos pueden unirse
entre sí, formando diferentes compuestos. Estos átomos que se unen pueden ser
iguales o distintos así tenemos que cuando los átomos se unen se dice que
forman enlaces.
Hay átomos que se atraen entre sí con mucha fuerza y se unen muy fuertemente y
otros que prácticamente no se atraen nada y no se unen.
Los átomos dependiendo de su naturaleza pueden
unirse entre sí formando enlaces.
Clasificación de la materia
La materia puede clasificarse en día
categorías principales

Sustancias puras
Son aquéllas cuya naturaleza y composición no varían sea
cual sea su estado.
Elementos: Son sustancias puras que no pueden
descomponerse en otras sustancias puras más sencillas por ningún procedimiento.
Ejemplo: Oxigeno (O) Litio (Li) Mercurio
(Ag) Nitrógeno (N)
Compuestos:
Son sustancias puras que están constituidas por 2 o más elementos combinados
en proporciones fijas y están representados mediante fórmulas químicas
Ejemplo: Agua (H20) Ácido clorhídrico (HCl) Hidróxido
de aluminio (Al (OH)3)
Mezclas
Se encuentran formadas por 2 o más sustancias puras y su
composición es variable.
Mezcla homogénea: Son mezclas en las que no se
pueden distinguir sus componentes a simple vista. Se las conoce también como
disoluciones.
Ejemplo: Disolución de sal en agua, el
aire, una aleación de oro y cobre.
Mezcla heterogénea: Son mezclas en las que se
pueden distinguir a los componentes a simple vista.
Ejemplo: Agua con aceite, granito, arena en
agua.
Las mezclas se pueden separar mediante distintos métodos de
separación dependiendo del estado de agregación en que se encuentren los
componentes de la mezcla
Estados de agregación
de la materia
En una sustancia o elemento se observa que modificando sus
condiciones de temperatura y presión pueden obtenerse diferentes estados. Se
los conoce como estados de agregación de la materia en relación con las fuerzas
de unión entre las partículas que la constituyen.
Así tenemos tres estados
Sólido
La estructura microscópica de los sólidos indica que posee
las siguientes propiedades
- Su forma y su volumen son fijos y no varían
- Son incompresibles
- No existe mucho espacio entre sus partículas
- Su fuerza de cohesión es elevada
- Su fuerza de repulsión es nula
- Su fluidez es baja o nula
Las partículas de los sólidos
pueden vibrar y vibraran más rápido cuanto mayor sea la temperatura
Liquido
La estructura microscópica de los líquidos indica que posee
las siguientes propiedades
- Su forma se adapta al recipiente que los contiene
- Su volumen es fijo
- Son poco compresibles
- La energía cinética y potencial son aproximadamente iguales
- Presentan fluidez y viscosidad
Las partículas de los líquidos
se mueven pero manteniéndose unidas al
conjunto. La atracción entre las partículas es intermedia
Gaseoso
Poseen las siguientes propiedades
- Su forma y su volumen no son definidos
- Su volumen es variable
- Su densidad es mucho menor que la de líquidos y solidos
- Su fuerza de cohesión es casi nula
- La energía cinética es mayor que la energía potencial
- Son expansibles y compresibles
Al aumentar la temperatura las
partículas se mueven más deprisa y chocan con más energía contra las paredes
del recipiente, por lo que aumenta la presión
También podemos encontrar otro estado de la materia que se
denomina plasma
Plasma
 Este estado se forma
bajo temperaturas y presiones extremadamente altas. Se lo considera un gas
ionizado porque en los átomos que lo componen los electrones se han alejado del
núcleo dejando aniones y cationes libres y separados entre sí. Esto lo
determina como un buen conductor de electricidad; tiene algunas características
como:
Este estado se forma
bajo temperaturas y presiones extremadamente altas. Se lo considera un gas
ionizado porque en los átomos que lo componen los electrones se han alejado del
núcleo dejando aniones y cationes libres y separados entre sí. Esto lo
determina como un buen conductor de electricidad; tiene algunas características
como:- Su forma y su volumen no es definido
- Bajo la influencia de un campo magnético puede formar estructuras como filamentos, rayos y capas dobles.
Calentar un gas puede ionizar
sus moléculas o átomos convirtiéndolo en
un plasma.
El sol es un ejemplo presente de
plasma en nuestro universo
El agua es la única sustancia
que puede hallarse de modo natural en los tres estados (solido, líquido,
gaseoso)
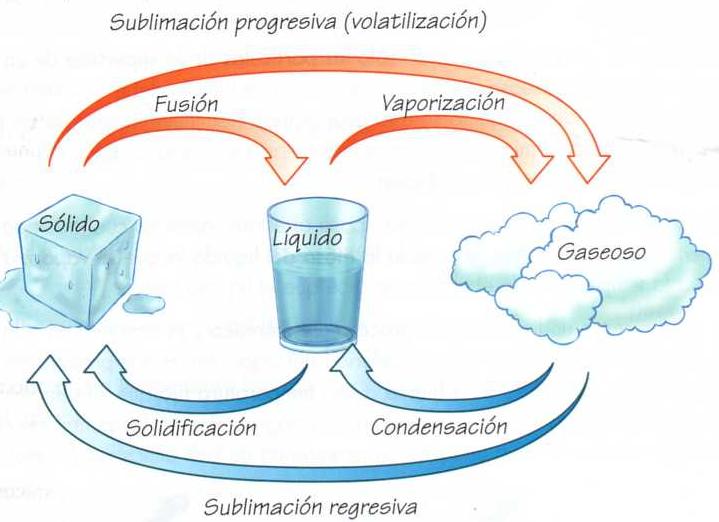
Los cuerpos pueden
cambiar de estado al variar la presión y la temperatura.
Ley de la
conservación de la materia
La masa de un sistema permanece invariable cualquiera que
sea la transformación que ocurra dentro de él; esto es, en términos químicos,
la masa de los cuerpos reaccionantes es igual a la masa de los productos en
reacción. Así fue enunciada en el año 1745, Mijaíl Lomonosov. En el mismo año,
y de manera independiente, el químico Antoine Lavoisier propone que “la materia
no se crea ni se destruye, sólo se transforma”. Es por esto que muchas veces la
ley de conservación de la materia es conocida como ley de Lavoisier-Lomonosov.
En el siguiente video se puede apreciar una explicación mas científica de lo que es la materia y sus influencias físicas y estados.
´
JUEGO INTERACTIVO

¿Está buscando un prestamista de préstamos positivo para solucionar su problema financiero? Entonces le gustaría que pedro ofreciera un préstamo, pedro me ofreciera un préstamo a una tasa de 3 roi y todo el proceso se desarrolló sin problemas como esperaba, puede enviarle un correo electrónico si necesita algún tipo de préstamos email: pedroloanss@gmail.com o whatsapp: +18632310632
ResponderEliminar